Содержание:
- 1 Прогрессирующая оссифицирующая фибродисплазия
- 1.1 Прогрессирующая оссифицирующая фибродисплазия (ФОП)
- 1.2 Характеристика заболевания
- 1.3 Как развивается
- 1.4 Диагностика
- 1.5 Прогрессирующая оссифицирующая фибродисплазия
- 1.6 Генетический аспект и будущее лечение
- 1.7 Как научиться жить с диагнозом прогрессирующая оссифицирующая фибродисплазия?
- 1.8 Что такое ФОП?
- 1.9 Причины заболевания
- 1.10 Симптоматика заболевания
- 1.11 Диагностика прогрессирующей оссифицирующей фибродисплазии
- 1.12 Методы лечения
- 1.13 Профилактические рекомендации и прогнозы
- 1.14 Чем опасно развитие оссифицирующей фибродисплазии?
- 1.15 Механизм развития и стадии
- 1.16 Провоцирующие факторы
- 1.17 Симптомы заболевания
- 1.18 Терапевтические мероприятия
- 1.19 Фибродисплазия
- 1.20 Оссифицирующая прогрессирующая фибродисплазия: опасность генетического наследования
- 1.21 Что представляет собой заболевание?
- 1.22 Причины о ссифицирующей прогрессирующей фибродисплазии
- 1.23 Характерные симптомы
- 1.24 Диагностика
- 1.25 Как лечить болезнь Мюнхеймера?
- 1.26 Чего нельзя делать и следует избегать?
- 1.27 Профилактика
- 1.28 Оссифицирующая фибродисплазия: неминуемая смерть в каменном теле
- 1.29 Что известно о болезни?
- 1.30 Стадии развития заболевания
- 1.31 Причины заболевания
- 1.32 Симптоматика и диагностирование
- 1.33 Генетические исследования
- 1.34 Как замедлить развитие болезни
- 1.35 Прогрессирующий оссифицирующий миозит и прогрессирующая оссифипирующая фибродисплазия
- 1.36 Фибродисплазия
- 1.37 Классификация
- 1.38 Симптоматика
- 1.39 Диагностика
- 1.40 Профилактика
Прогрессирующая оссифицирующая фибродисплазия
Прогрессирующая оссифицирующая фибродисплазия (ФОП)
Фибродисплазия относится к редчайшему заболеванию, которое возникает в результате мутации определенного гена. На сегодняшний день в мире зарегистрировано 600 человек, страдающих от него. Патология характеризуется окостенением мышц, связок, сухожилий. Сначала поражается позвоночник, далее страдают другие кости организма.
Характеристика заболевания
Оссифицирующая фибродисплазия (ФОП) по МКБ 10 имеет номер М61.1, возникает из-за генетических мутаций, в результате видоизменения гена ACVR1. Известны случаи, когда поражаются несколько членов семьи, которые находятся в кровном родстве, братья и сестры. Встречается передача заболевания от одного поколения к другому, от отцов к детям.
Данная патология носит название болезни «второго скелета». Прогрессирующую фибродисплазию провоцируют воспалительные процессы мышц, сухожилий, связок, мягких тканей, по истечении времени приводя к окостенению.

Не следует путать данное заболевание с фиброзной дисплазией, при котором происходит замещение здоровой ткани кости на включение костной трабекулы. Фиброзная дисплазия относится к разряду опухолевых состояний, но не является раковой опухолью. Часто происходит перерождение в доброкачественное новообразование, онкология встречается редко.
У пациентов любой ушиб, небольшая ранка не вылечивается, на месте повреждения происходит образование костной ткани.
У новорожденного почти полностью определяется наличие заболевания, от которого одинаково страдают и девочки, и мальчики. Оно обнаруживается загнутым внутрь большим пальцем ноги и отсутствием сустава. Патология проявляется в первые 10 лет жизни больного, характеризуется внезапностью. Нижние конечности страдают в последнюю очередь.
Насколько быстро будет развиваться болезнь установить невозможно. Так как это зависит от количества полученных травм и перенесенных оперативных вмешательств.
Бывают случаи, когда врачи путают оссифицирующую фибродисплазию с онкологией, которая приводит к формированию костных образований. После их удаления происходит резкое усугубление ситуации и ускоренное развитие патологии.
Как развивается
Оссифицирующая фибродисплазия развивается по стадиям:
- На первой стадии образуется небольшой воспалительный очаг,
- На второй стадии патология начинает прогрессировать, воспаление вовлекается в ткани, расположенные около воспаленного места,
- На третьей стадии образуются бессосудистые уплотнения,
- Далее формируется хрящеобразование,
- Завершающей стадией является окостенение.
Оссифицирующая фибродисплазия начинает свое формирование еще в период внутриутробного развития, в результате изменения гена, расположенного во второй хромосоме. Из-за чего происходит мутация формы белка, отвечающего за развитие костной ткани.
Гетеротопические фибродисплазийные очаги обычно формируются в местах повреждения мягкой ткани, ожогов, укусов насекомых, порезов, ушибов. В данной области обнаруживается много лейкоцитов, являющихся фактором иммунного, воспалительного процесса.
Имеются пациенты, которые являются носителями гена, и при определенных обстоятельствах заболевание начинает прогрессировать. На скорость его проникновения оказывает воздействие активность гена. К провоцирующим факторам относятся:
- Хирургические вмешательства,
- Вакцинирование,
- Травмирование кожного покрова,
- Вирусная инфекция
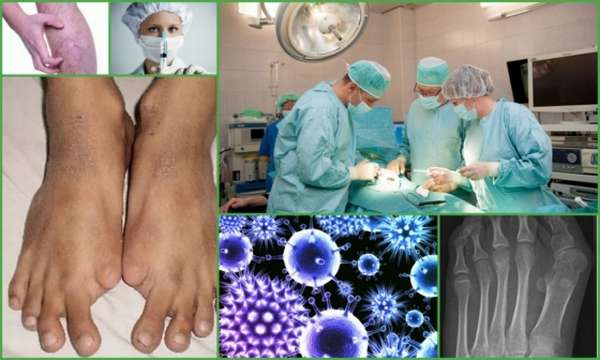
Оссифицирующая фибродисплазия редко начинает развиваться сразу же после рождения ребенка. Врачи обращают внимание на нарушение сформированности пальчиков на ногах и руках. Никаких других внешних проявлений не наблюдается.
Оссификация начинается внезапно, порой без наличия объективной причины. Возраст ребенка может быть от 2-3 месяцев до нескольких лет. Чаще прогрессирование происходит в первые пять лет жизни. Симптомами заболевания считаются:
- Ранняя симптоматика проявляется формированием небольшого уплотнения, размером до 3 мм,
- При прогрессировании уплотнение увеличивается до 10 см,
- При пальпации наблюдается болезненность, иногда покраснение,
- Походка у пациента приобретает неуверенность, скованность,
- На лице отсутствуют какие-либо эмоции,
- Происходит уменьшение объема движений, что имеет связь с появлением новых уплотнений, приводя к полной обездвиженности,
- При прощупывании появляются боли в ногах,
- Нарушается чувствительность,
- Происходят сбои функционирования внутренних органов.
Наиболее очевидной клинической картиной заболевания считают окостенение мягкой ткани. Но возможно проявление следующих дефектов, говорящих о наличии оссифицирующей фибродисплазии:
- Короткий по отношении к остальным большой палец ноги, характеризующийся изогнутостью внутрь,
- Дефект в шейном отделе позвоночника,
- Короткий большой палец рук,
- Отставание в развитии,
- Глухота,
- Облысение,
- Искривление пятого пальца ног,
- Кривошея,
- Сколиоз,
- Тугая подвижность костного сочленения.
Известны случаи, когда уплотнения самостоятельно рассасываются, но в последствии образуются снова. После чего через 2-3 недели происходит их окостенение, в результате которого стает невозможным дальнейшее их рассасывание. У взрослого пациента прогрессирующая болезнь Мюнхеймера приводит к слиянию десятков очагов. Что в последствии вызывает глубокую инвалидизацию и летальный исход.

Диагностика
Диагностирование оссифицирующей фибродисплазии возможно после окончания форсированного костеобразования, которое происходит с момента рождения до 14 лет. Часто заболевание обнаруживается спустя 2 года после его развития. Диагностирование проводится следующими методами:
- Внешним осмотром,
- Рентгенографией,
- Генетической консультацией.
Во время внешнего осмотра у детей до 10-летнего возраста обнаруживаются многочисленные уплотнения, располагающиеся в разных частях тела. В более старшем возрасте определяется пониженная суставная подвижность, искривленный позвоночник, гетеротропические оссификационные очаги. Уплотнения можно увидеть даже невооруженным глазом.
В исключительных случаях может потребоваться гистологическое исследование, но оно проводится редко, чтобы исключить появления новых уплотнений.
Рентгенография полезна на начальном этапе оссифицирующе патологии, поскольку позволяет выявить дисплазию кости, клинодактилию. На поздних стадиях костные уплотнения появляются в мышечной ткани, сухожилиях. Если болезнь зашла далеко, то на рентгеновском снимке не возможно визуализировать внутренние органы.

На сегодняшний день не существует методов, вылечивающих прогрессирующую оссифицирующую фибродисплазию. Но американскими учеными активно проводятся исследования гена, который влияет на развитие патологии. Разрабатываются генные блокаторы, которые способны остановить процесс мутации. Восстанавливается нормальное синтезирование белков за счет нейтрализации мутировавшего гена.
Для лечения оссифицирующей фибродисплазии используют следующие лекарственные препараты:
- Этидронат, который замедляет формирование костной ткани. Но ударная доза средства не только оказывает воздействие на патологические кости, но и приводит к разрушению основного скелета,
- Лекарственные средства, основанные на Ламидроновой кислоте, схожи своим действием с предыдущими препаратами, но не так активно влияют на основные кости,
- Преднизолон оказывает мощное противовоспалительное действие, снижает боль, устраняет опухоли. Курс лечения данным средством не должен превышать 2 недель. Иначе происходит ускорение роста костной ткани, подавление иммунитета, ухудшение зрения,
- Целебрекс замедляет воспаление,
- Метаксалон используется для снижения вспышек заболевания, приводит к ослаблению спазмов.
Улучшает состояние больных, страдающих от фибродисплазии, иммунотерапия Интерфероном. Ее действие направлено на замедление прогресса патологии, уменьшение числа уплотнений. Для облегчения самочувствия пациентам назначают обезболивающие и седативные препараты.
Наибольшую безопасность для больных представляет оперативное вмешательство по поводу устранения уплотнений и костного разрастания. После процедуры обнаруживается усиление процесса окостенения.
На начальном этапе оссифицирующей патологии больному назначается электрофорез на основе йодида калия. Противопоказаны пациентам УВЧ, массажи, парафинотерапия.
Людям с оссифицирующей фибродисплазией необходимо исключение хирургического вмешательства, любых видов инъекций для минимизации риска возникновения новых травм.
Данное заболевание имеет неблагоприятный исход. На продолжительность жизни больных оказывают влияние создание условий, исключающих травм, увечий, инфекционных заболеваний.
Прогрессирующая оссифицирующая фибродисплазия
Дети, рожденные с Фибродисплазией, отличаются характерной патологией большого пальца ноги — одна или несколько фаланг пальца искривлены вовнутрь и иногда в нем не хватает сустава. Этот палец и дает 95 % — ную вероятность заболевания у ребенка. Также болезнь характеризуется обострениями, как правило, без видимых причин. Обострения бывают нескольких видов, самое распространенное — появление под кожей ребенка уплотнений размером от одного до десяти сантиметров неопределимого характера, на шее, спине, предплечьях в возрасте до 10 лет, в любом другом месте в более старшем возрасте. Одним из признаков является отек мягких тканей головы, как при незначительном повреждении (ушиб, укус насекомого, царапина), так и при сильных травмах. Отек не спадает до месяца, не реагирует ни на какую медикаментозную терапию.На месте уплотнений могут возникать оссификации, она не нуждается ни в каком лечении и не поддается никаким препаратам. Болезнь часто путают с раком и другими заболеваниями, подобные затвердения пытаются удалять, что приводит к ещё более бурному росту «лишних» костей,и является основной причиной инвалидизации страдающих этим заболеванием на данный момент.
Вспышки ФОП являются спорадическими и непредсказуемыми, и есть огромная разница в каждом индивидуальном проявлении. Несколько базовых научных исследований подтвердили невозможность предсказать начало, силу, последствия и продолжительность обострения ФОП, хотя особенности анатомических патологий уже были описаны. Редкость ФОП и ее непредсказуемая природа делает чрезвычайно трудным оценку эффективности любого терапевтического вмешательства, факт, признанный 1918 году врачом Джулиус Розенстирн :
«Болезнь развивается со всеми видами средств и альтернатив дефектного метаболизма; каждое отдельное терапевтическое вмешательство с более или менее отмеченным успехом, наблюдаемым исключительно его оригинальным автором, в будущем раскритиковывается любым последователем. Во многих случаях, признаки болезни исчезают часто спонтанно, таким образом, терапевтический эффект (любого лечения) не может быть полностью подтвержден своей эффективностью.»
Эти слова звучат правдоподобно и сегодня, несмотря на то, что они были написаны почти столетие назад. В настоящее время не существует никаких доказанных эффективных методов профилактики или лечения ФОП. С открытием гена ФОП стало возможным понимание патогенеза заболевания. Перспективной является непосредственная работа с геномом, но в настоящее время данные методы лечения находятся лишь на стадии предварительных лабораторных исследований и не применяются в клинической практике.
Генетический аспект и будущее лечение
В 2006 году исследовательская группа из Университета штата Пенсильвания открыла ген, мутация в котором приводит к этому заболеванию. Чтобы идентифицировать хромосомное местоположение для гена ФОП, консервативной связки всего генома, анализ проводился с помощью наблюдения за пятью семьями с самыми однозначными особенностями ФОП. Этот подход идентифицировал связку ФОП к хромосоме 2q23-24.
Генотерапия: В настоящее время идет работа над генными блокаторами мутации в гене ACVR1/ALK2.В декабре 2012 завершены с успехом опыты по лечению гетеротопической оссификации лабораторным мышам.Препарат показал свою действенность как в генетически обусловленной так и в посттравматической оссификации. В течение 2013 года начнутся испытания препарата в первой фокус — группе пациентов ФОП. Золотой стандарт для всех исследований нового препарата — тройной слепой перекрестный метод с применением плацебо, но такие исследования будет достаточно трудно провести при ФОП, ввиду малого количества пациентов с болезнью в уже развитой стадии, неоднозначным патогенезом болезни, а также большой разницей в проявлениях обострений у пациентов. Ввиду того, что фибродисплазия является чрезвычайно редким заболеванием, с разной тяжестью проявлений, экспериментальным методам лечения, предстоит пройти серьёзную оценку на предмет дозировки и продолжительности курса.
- [3] — Информационный сайт для страдающих заболеванием и их врачей
- The International FOP Association
- [4]
- [5]
- Rare ‘stone man’ gene that changes muscle into bone -News-World-US & Americas-TimesOnline. Проверено 2 июня 2007.
Frederik Kaplan The medical management of Fibrodysplasia Ossificans Progressiva: current treatment considerations |2008
Как научиться жить с диагнозом прогрессирующая оссифицирующая фибродисплазия?
Прогрессирующая оссифицирующая фибродисплазия или болезнь Мюнхеймера — одно из самых редких заболеваний опорно-двигательного аппарата, вследствие которого происходит утрата дееспособности пациента за счет окостенения соединительных тканей и приводящее к преждевременной смерти больного.

Безболезненная, уникальная методика доктора Бобыря
Дешевле, чем мануальная терапия
Получайте пропуск и приезжайте к нам!
Только с 1 по 10 июня! Записывайтесь сейчас!
Исторические данные и клиническая картина
Случаи выявления диагноза фиксируются один на два миллиона. Один из самых первых пациентов, пораженных данным заболеванием, был зарегистрирован в 1648 году. На сегодняшний день насчитывается не более 300 случаев.
Источником возникновения недуга выступает мутирование клеток на генетическом уровне.
- Первое, на что нужно обратить внимание — это пальцы ног. У больного человека они будут искривленными.
- Также от заболевания страдают позвонки шейного отдела, в частности со второго по седьмой.
Прогрессирующая оссифицирующая фибродисплазия (ПОФ) носит наследственный характер — это врождённое заболевание. При этом оно не стоит на месте, а постоянно прогрессирует, его течение невозможно остановить. Современной науке, к сожалению, пока не удалось обнаружить действенные методы борьбы. С раннего детства проявляются признаки болезни в виде нарушений в опорно-двигательном аппарате, приводящие ребёнка к инвалидизации. В основной массе такие больные умирают в молодом возрасте, но в истории есть люди, дожившие до глубокой старости. Как правило, это единичные случаи. Причём причиной смерти служит не сама фибродисплазия, а заболевания, появившиеся на фоне окостенения организма. Чаще всего это легочная инфекция, возникающая из-за недостаточной вентиляции. Иногда смертельный исход наступает в результате истощения организма из-за окостенения глотательной мускулатуры.
Болезнь берет начало с воспалительного процесса, возникающего в сухожилиях, мышцах, связках, фасциях и мягких тканях организма. Со временем за счёт кальцифицирования их структура уплотняется и костенеет. Отсюда и произошло ещё одно название заболевания — «Болезнь второго скелета».
Симптомы фибродисплазии
- Главным симптомом фибродисплазии у новорождённых детей является искривление больших пальцев обеих ног, а если быть точнее, то они загнуты во внутрь, в сторону расположенного рядом пальца. Помимо этого, встречаются случаи отсутствия суставов на них.
- Следующим отличительным признаком является отечность мягких тканей головы, образовавшаяся после ушиба либо другого повреждения. В этом случае даже при медикаментозном вмешательстве отечность не спадает в течение месяца и более. Лечение бесполезно, так как уплотнения уже являются патологическими окостенениями.
На каком этапе течения болезни произойдёт обострение, и что влияет на её развитие, предугадать невозможно. Изменения, происходящие в организме, всегда отличаются друг от друга. Но, наиболее частые из них — это уплотнения под кожей размером не более 10-ти см, которые достаточно просто определяются на ощупь. Пальпация наростов будет доставлять неприятные болезненные ощущения. У детей младшего школьного возраста и моложе концентрация оссификатов приходится на область спины, шеи и предплечий. Ситуация со временем осложняется тугоподвижностью суставов, проявлением кривошеи, деформацией грудной клетки. У взрослых людей уплотненные образования могут прощупываться в любом месте.
Нередко фибродисплазию ошибочно принимают за раковую опухоль, так как при ней тоже происходит отечность тканей. Но, при попытке удаления оссификатов ситуация только усугубляется, провоцируя рост новых образований.
Проведение лабораторного обследования и профилактика заболевания
При обнаружении вышеперечисленных признаков прогрессирующей оссифицирующей фибродисплазии необходимо незамедлительно обратиться к специалисту и ни в коем случае не заниматься самолечением. Врач назначит пройти генетическое тестирование, по результатам которого предполагаемый диагноз либо подтвердится, либо будет опровергнут.
Сегодня молекулярно-генетическое исследование входит в перечень услуг большинства диагностических центров. Это несложная процедура и осуществляется путем забора крови с утра на голодный желудок. Важно учесть, что за сутки до анализа нельзя принимать алкогольные напитки. Результаты тестирования будут готовы примерно через семь дней.
Лишь только при обнаружении мутирующего гена ACVR1, отвечающего за формирование и восстановление костной системы, врач имеет право подтвердить диагноз.
К сожалению, данная патология неизлечима и единственный выход из ситуации — это постоянное проведение профилактических мероприятий с целью недопущения костных новообразований.
Люди, страдающие этим недугом, должны быть крайне аккуратны в обыденной жизни, избегая ушибов, царапин, травм и даже простудных и воспалительных заболеваний. Так как эти факторы могут отрицательно повлиять на течение болезни и привести к появлению новых костных уплотнений.
Лечение фибродисплазии в перспективе
Американские исследователи при университете Томаса Джефферсона создали новый препарат, блокирующий мутацию гена ACVR1/ALK2, и опробовали его на лабораторных мышах. Он оказал эффективное воздействие на ход лечения гетеротопической оссификации: прогресс заболевания приостановился, и снизились воспалительные процессы в поврежденных заболеванием тканях. Изобретенное средство может противостоять «болезни второго скелета», образовавшейся на фоне полученных повреждений и имеющей наследственный характер. В ближайшие три-пять лет американские учёные-генетики будут продолжать тестировать препарат и совершенствовать его возможности. За более короткий промежуток времени провести исследования не представляется возможным, так как синдром каменного человека крайне редкое явление, и каждый случай уникален.
Что такое ФОП?
Тяжелая генетическая аномалия, результатом которой является нарушение обмена в тканях мышц и связок, известна как прогрессирующая оссифицирующая фибродисплазия. Признаки этой редкой болезни проявляются в виде уплотнений в области шеи, спины и конечностей, возникающие в мягких тканях и способствующие кальцинированию. Со временем происходят серьезные деформации позвоночника, ограничивающие подвижность пациентов, что постепенно приводит к инвалидности.

Причины заболевания
Источник возникновения патологии — мутирование гена ACVR1, который проявляется сразу после рождения ребенка в виде искривлений больших пальцев ног, а также нарушениями в позвоночнике между вторым и седьмым позвонками. Также одним из возможных факторов развития болезни считаются травмы. В основе ФОП лежат воспалительные процессы, запускающие механизм окостенения в мышцах, сухожилиях и мягких тканях, прогрессирующий со временем, вследствие чего происходит дальнейшее ограничение подвижности пациента.
Симптоматика заболевания
Основными проявлениями недуга считаются:
- воспалительные явления в мышцах:
- скелетизация мягких тканей.
 Искривленность пальца может свидетельствовать о наличии болезни.
Искривленность пальца может свидетельствовать о наличии болезни.
Вспомогательные симптомы представлены такими дефектами:
- укороченный большой палец на ноге;
- короткопалость на кисти;
- искривленность пятого пальца;
- патологии шейных позвонков;
- укорочение и расширение в шейках бедренных и плечевых костей;
- облысение, глухота, отставание в развитии.
Формирование костных образований происходит из-за реакции организма на воспалительные процессы — кости начинают расти там, где их не должно быть. Патологические нарушения в опорно-двигательном аппарате становятся причиной сдавливания внутренних органов человека. При этом происходит осложнение процесса дыхания, нарушается нормальное функционирование сердца и даже блокируется работа жевательных мышц. В итоге происходит полное обездвиживание пациента, который не может выполнять обычные функции без помощи посторонних, что приводит к инвалидизации. Больные «каменной болезнью» часто умирают в молодом возрасте.
Диагностика прогрессирующей оссифицирующей фибродисплазии
Определить заболевание можно на основании внешнего осмотра больного, а также генетических и рентгенологических исследований. Основным способом диагностики заболевания остается исследование c помощью рентгена. Именно так можно разглядеть очаги распространения патологии, которые обычно располагаются на плечах и в области грудной клетки. Помимо этого, признаком начала развития фибродисплазии могут быть аномалии шейного отдела позвоночника. При рентгенографическом исследовании можно определить степень тяжести заболевания.
Различают следующие стадии:
- Инфильтрация. Представлена разрастанием дегенеративных тканей и некоторыми патологическими изменениями в мышцах.
- Фиброзная индурация. Характерна процессом рубцевания и началом атрофии мышечных структур.
- Окостенение. Формирование костной ткани, на снимках уже можно четко увидеть большие участки с окостеневшими мышцами, позвоночник становится похожим на бамбук.
При этом результаты анализов мочи, крови и минерального обмена не выявляют каких-либо отклонений от нормы. Генетическое исследование необходимо для постановки правильного диагноза, так как зачастую деформирование первых пальцев стоп ошибочно принимается за вальгусную деформацию. Потеря времени чревата осложнениями в дальнейшем лечении.
Иногда проводится биопсия, но многие врачи считают процедуру опасной. Предполагается, что она вызовет дополнительное поражение тканей, приводящее к окостенению травмированного участка.
Методы лечения
На начальных стадиях болезни применяют глюкокортикостероиды, которые уменьшают разрушительное воздействие недуга на организм и облегчают процессы жизнедеятельности больных. К полному выздоровлению прием данных лекарств привести не может. Существуют медикаментозные средства, способные затормозить развитие болезни. Среди прочих препаратов можно выделить «Интерферон-g», длительное применение которого способствует уменьшению мышечных уплотнений. Кроме того, больным показаны к применению биофосфонаты и этилендиаминтетрауксусная кислота.
Новый препарат «Паловаротен» применяют для блокирования очагов разрастания костной ткани. А «Интерферон лейкоцитарный» при длительном применении, способен снизить количество костных образований. Своевременная диагностика позволит вовремя распознать болезнь и начать лечение глюкокортикостероидами, что продлит жизнь пациента и улучшит ее качество.
Профилактические рекомендации и прогнозы
Больным ФОП следует избегать травм мягких тканей, переохлаждения и перегревания организма, общения с больными ОРВИ, любого рода инъекций и хирургических вмешательств. Такие профилактические меры способны затормозить процесс развития заболевания. Прогноз для страдающих этим недугом пока остается неутешительным. Прогрессирующая фибродисплазия постепенно приводит к окостенению все больших участков тела. Лекарственная терапия способна замедлить эти процессы и облегчить жизнедеятельность больных.
Чем опасно развитие оссифицирующей фибродисплазии?
Фибродисплазия оссифицирующая прогрессирующая — патологическое состояние, при котором наблюдается постоянное окостенение мягких тканей опорно-двигательного аппарата. Заболевание захватывает мышечные и соединительные волокна, сухожилия и связки. Оссифицирующая фибродисплазия считается скелетной аномалией врожденного характера. Болезнь отличается спонтанным возникновением обострений, при которых мягкие ткани превращаются в костные.

Механизм развития и стадии
В прошлом данное заболевание в медицине имело название «болезнь второго скелета» или оссифицирующий миозит. Недавние исследования показали, что данные термины не совсем точно отражают патологические изменения, возникающие в организме при ФОП.
Это заболевание подвергается тщательному изучению в течение нескольких столетий. Первые сведения о пациентах с фибродисплазией появились в 17-м веке. Окостенение скелетных мышц начинается в первые дни жизни. Патологический процесс распространяется сверху вниз, на ранних стадиях поражая шейный и грудной отделы. Окостенение затрагивает даже жевательные мышцы, из-за чего пациенты умирают от истощения.
 Скорость снижения двигательной активности не зависит от времени появления первых симптомов. Любой воспалительный процесс у человека, страдающего фибродисплазией, приводит к обострению и быстрому прогрессированию заболевания. Пораженные клетки проникают в мышечные ткани, ускоряя процессы их окостенения. В период дозревания фиброзные волокна образуют лишенные сосудов уплотнения. Превратившиеся в хрящи ткани вступают в процесс окостенения.
Скорость снижения двигательной активности не зависит от времени появления первых симптомов. Любой воспалительный процесс у человека, страдающего фибродисплазией, приводит к обострению и быстрому прогрессированию заболевания. Пораженные клетки проникают в мышечные ткани, ускоряя процессы их окостенения. В период дозревания фиброзные волокна образуют лишенные сосудов уплотнения. Превратившиеся в хрящи ткани вступают в процесс окостенения.
Фибродисплазия развивается в течение нескольких стадий:
- Началом патологического процесса считают возникновение локального воспаления. По мере развития заболевания оно охватывает окружающие первичный очаг ткани.
- На следующей стадии возникают бессосудистые уплотнения, после чего происходит образование хрящей.
- Последней стадией считается оссификация.
Болезнь Мюнхеймера может поражать различные отделы опорно-двигательного аппарата, окостенение в них происходит с разной скоростью. Патологические изменения, происходящие в организме при фибродисплазии, схожи с образованием костей у эмбриона. Основным отличием является отсутствие воспалительного процесса во втором случае.
Эти признаки считаются условными, ведь проведение биопсии больным фибродисплазией запрещено.
Провоцирующие факторы
 Причины, способствующие окостенению мягких тканей, не определены. Однако специалисты занимаются поиском ответа на этот вопрос. Каких-либо половых или расовых факторов, повышающих риск развития фибродисплазии, не обнаружено.
Причины, способствующие окостенению мягких тканей, не определены. Однако специалисты занимаются поиском ответа на этот вопрос. Каких-либо половых или расовых факторов, повышающих риск развития фибродисплазии, не обнаружено.
Плохая наследственность играет здесь не последнюю роль. Оссифицирующий миозит считается распространенным патологическим процессом, которому свойственна различная активность генов. В большинстве случаев заболевание обнаруживается лишь у одного из членов семьи, однако возможна его передача от родителей детям.
Симптомы заболевания
Характерными признаками ФОП считаются воспалительные процессы в мягких тканях и гетеротопическая оссификация. Вновь образующиеся кости практически не отличаются от уже имеющихся. Окостенение мягких тканей способствует развитию мышечной слабости, дистрофических нарушений и сращения суставов. Не выявлено факторов, под воздействием которых окостенение приобретает локальный характер либо распространяется по всему организму.

Фото. Фибродисплазия шеи
Симптомы ФОП представляют собой не только оссификацию мягких тканей, но и различные аномалии развития. Наиболее распространенными являются:
- короткопалость стоп;
- гипоплазия фаланг кистей;
- клинодактилия пятого пальца; и
- скривление шейного отдела позвоночника, которое можно увидеть на фото;
- укорочение и расширение плечевых и бедренных костей.
Существует высокий риск развития тугоухости, аллопеции, гипогонадизма и отставания в физическом развитии. Практически у всех пациентов обнаруживаются признаки кривошеи, сколиоза и снижения подвижности суставов.
 Заболевание обычно обнаруживается на стадии активной оссификации в скелетных тканях. Возникает она в детском или подростковом возрасте. Первые подозрения у врача могут появиться при обследовании 3-летнего ребенка, страдающего фибродисплазией. Врожденные же аномалии обнаруживаются в первые дни жизни. Заболевание крайне редко диагностируется на ранних стадиях. Причиной тому является малоизвестный механизм развития патологических изменений. Не каждый специалист может догадаться, из-за чего появилась такая аномалия, как короткопалость стопы.
Заболевание обычно обнаруживается на стадии активной оссификации в скелетных тканях. Возникает она в детском или подростковом возрасте. Первые подозрения у врача могут появиться при обследовании 3-летнего ребенка, страдающего фибродисплазией. Врожденные же аномалии обнаруживаются в первые дни жизни. Заболевание крайне редко диагностируется на ранних стадиях. Причиной тому является малоизвестный механизм развития патологических изменений. Не каждый специалист может догадаться, из-за чего появилась такая аномалия, как короткопалость стопы.
В настоящее время наиболее важную роль играют генетические исследования. Основной находкой в этой области считается обнаружение мутации BMP4-гена и его РНК у 70% пациентов. ВМР-4 — белковое соединение, ответственное за формирование костных тканей и заживление переломов. Оно содержит гены, повреждение которых может привести к развитию фибродисплазии.
Однако даже в 21-м веке точные причины возникновения заболевания остаются невыясненными. Специалисты предполагают, что фибродисплазия закладывается на генетическом уровне. Существует вероятность того, что оссифицирующий миозит вызывается мутацией нескольких генов.

Терапевтические мероприятия
Так как причины возникновения фибродисплазии выявить невозможно, не удается разработать эффективную схему лечения. Однако существуют препараты, способные замедлить развитие патологического процесса:
- Наиболее часто применяются интерфероны. Длительное введение этих препаратов препятствует образованию мышечных и подкожных уплотнений.
- Дополнительно назначаются биофосфонаты и этилендиаминтетрауксусная кислота.
Вторичная профилактика оссифицирующей фибродисплазии заключается в отказе от хирургических вмешательств и уколов, снижении риска возникновения травм.
Фибродисплазия
Фибродисплазия оссифицирующая прогрессирующая (оссифицирующий миозит, параоссальная гетеротопическая оссификация, болезнь Мюнхеймера) — редчайшее заболевание (1 заболевший на 2000000), возникающее в результате мутацией гена ACVR1, и проявляющееся врожденными дефектами развития — прежде всего искривленными большими пальцами стоп и нарушениями в шейном отделе позвоночника на уровне позвонков с2 — с7. Заболевание относится к врожденной наследственной патологии с аутосомно — доминантным типом наследования. Оно характеризуется неуклонно прогрессирующим течением, приводит к значительным нарушениям функционального состояния опорно-двигательного аппарата, глубокой инвалидизации больных и преждевременной их смерти, причем преимущественно в детском и молодом возрасте. Основу фибродисплазии составляет формирование воспалительных процессов всухожилиях, связках, фасциях, подкожных тканях и мышцах, что в конечном итоге приводит к их кальцификации и окостенению. Болезнь еще называют «Болезнь второго скелета», так как по сути, там где в организме должны происходить штатные противовоспалительные процессы, начинается рост кости.

Дети, рожденные с Фибродисплазией, отличаются характерной патологией большого пальца ноги — клинодактилией — он как бы загнут внутрь и иногда в нем не хватает сустава. Этот палец и дает 95 % — ную вероятность заболевания у ребенка. Также болезнь характеризуется обострениями, как правило, без видимых причин. Обострения бывают нескольких видов, самое распространенное — появление под кожей ребенка уплотнений размером от одного до десяти сантиметров неопределимого характера, на шее, спине, предплечьях в возрасте до 10 лет, в любом другом месте в более старшем возрасте. Одним из признаков является отек мягких тканей головы, как при незначительном повреждении (ушиб, укус насекомого, царапина), так и при сильных травмах. Отек не спадает до месяца, не реагирует ни на какую медикаментозную терапию. Уплотнения — это оссификаты, они не нуждаются ни в каком лечении и не поддаются никаким препаратам. Болезнь часто путают с раком и другими заболеваниями, подобные затвердения пытаются удалять, что приводит к еще более бурному росту «лишних» костей,и является основной причиной инвалидизации страдающих этим заболеванием на данный момент.
 клинодактилия пальцев рук
клинодактилия пальцев рук

На страницы британских газет попала история 13-летней девочки, которую исключительно редкое заболевание постепенно превращает в «живую статую».
Юная британка страдает прогрессирующей оссифицирующей фибродисплазией – генетической мутацией, при которой в месте любого, даже незначительного повреждения волокнистых тканей (мышц, связок, сухожилий) наблюдается рост костной ткани. В результате этого костные разрастания постепенно приводят к нарушению движений во всех суставах вплоть до полной неподвижности. Заболевание встречается чрезвычайно редко – во всем мире насчитывается около 600 случаев.
Фибродисплазия уже зафиксировала руки Шони Нэммок в полусогнутом положении и значительно снизила подвижность ее позвоночника. Диагноз был поставлен в прошлом году, когда после падения на спину в месте ушиба появилось плотное болезненное образование. Капельница, поставленная девочке до подтверждения диагноза, вызвала разрастание костной ткани, обездвижившее ее левый локтевой сустав.
По словам Шони, ей приходится выходить из класса на несколько минут раньше перерыва, чтобы избежать случайных толчков в коридоре. Во время прогулок друзья заслоняют ее от прохожих.
Эксперт по прогрессирующей оссифицирующей фибродисплазии Фредерик Каплан рассказал, что заболевание со временем буквально формирует второй скелет, который сковывает тело больного, не давая ему двигаться.
Лечения этой редкой болезни в настоящее время не существует. Единственной надеждой для Шони остается исследовательский проект Оксфордского университета, созданный для разработки методов борьбы с фибродисплазией.

Оссифицирующая прогрессирующая фибродисплазия: опасность генетического наследования
 В природе не существует идеального человеческого генома. У каждого из нас есть от одного до шести генов, которые повреждены. Однако большинство представителей человеческого рода вполне здоровы. Это явление связано с тем, что дефект генов не проявляется, пребывает в рецессивном состоянии.
В природе не существует идеального человеческого генома. У каждого из нас есть от одного до шести генов, которые повреждены. Однако большинство представителей человеческого рода вполне здоровы. Это явление связано с тем, что дефект генов не проявляется, пребывает в рецессивном состоянии.
Совсем другое дело, если «больные гены» составляют доминанту наследования. Они будут в любом сочетании кодировать патологические механизмы или качества. К таким наследственным патологиям относится оссифицирующая прогрессирующая фибродисплазия.
Что представляет собой заболевание?
Фибродисплазией называется заболевание, имеющее генетическую природу. Оно связано с патологическим окостенением мягких тканей, чаще соединительных. В деформационные процессы могут вовлекаться мышечные фасции и связки. Дефект соответствующего гена дает проявление в фенотипе уже в раннем возрасте. Болезнь встречается очень редко. Ее еще называют болезнью Мюнхеймера.
Причины о ссифицирующей прогрессирующей фибродисплазии
Заболевание носит наследственный характер. Его передаче потомству способствует патология аутосом (соматических хромосом). При размножении клеток дефект считывается и копируется, что дает возможность его проявлению у детей больных родителей или носителей гена.
Наследование гена, отвечающего за фибродисплазию, происходит за доминантным типом. Это означает, что в случае сочетания у ребенка здорового гена и «бракованного» второй будет подавлять здоровый и преобладать над ним.
Как результат плохой наследственности у детей происходит:
- диффузное воспаление мышц, костей и связок;
- отложение кальция в мягких тканях;
- их окостенение;
- расстройство функции костно-мышечной системы;
- постепенно прогрессирующая инвалидизация;
- наступление летального исхода в раннем или молодом возрасте.
Характерные симптомы
Патология сопровождается определенными признаками, которые характерны для заболевания:
- клинодактилией – изменением анатомического состояния первого пальца стопы с отсутствием одного из суставов;
- обострением в виде появления подкожных уплотнений на шее и спине;
- отечными явлениями тканей головы на фоне незначительного травмирования;
- длительным сохранением отека;
- переходом воспалительного процесса в оссификацию;
- усилением роста и увеличением количества оссификатов после хирургических вмешательств;
- инвалидизацией после каких-либо терапевтических и хирургических процедур.
Киста Бейкера коленного сустава — что это за патология? Узнайте из этой статьи.
Что такое коксартроз тазобедренного сустава, и как его правильно лечить?
Диагностика
С помощью обычных диагностических процедур невозможно установить диагноз фибродисплазия. Поэтому необходимо генетическое исследование. Аномалию пальцев используют для дополнения общей картины патологического процесса.
В связи с очень редкими случаями заболевания изучить и диагностировать фибродисплазию удается не всегда. По течению заболевание может напоминать онкопатологию и фиброматоз.
Ошибки в диагностике и некорректное лечение ведут к инвалидизации пациента.
Как лечить болезнь Мюнхеймера?
 Цифры заболеваемости фибродисплазией весьма ничтожны. Лишь около восьмиста человек по всему миру имеют такую наследственную патологию. Медицинские институты проводят ряд исследований, но до сих пор никому не удалось эффективно решить генетическую загадку.
Цифры заболеваемости фибродисплазией весьма ничтожны. Лишь около восьмиста человек по всему миру имеют такую наследственную патологию. Медицинские институты проводят ряд исследований, но до сих пор никому не удалось эффективно решить генетическую загадку.
Медикаментозное лечение заключается в назначении:
- седативных препаратов;
- обезболивающих;
- другой симптоматической терапии.
Народные и хирургические методы на сегодняшний день являются бессильными против заболевания. Но надежда все же есть, поскольку мировые генетики нашли закономерность между определенными генетическими аномалиями и появлением болезни. На сегодняшний день клинические испытания продолжаются.
Чего нельзя делать и следует избегать?
- Самую большую опасность для больного фибродисплазией представляют операции по удалению кальцинатов и патологических костных разрастаний.
- Вообще любое нарушение целостности тканей вызывает резкую активацию патологического роста костных структур. Поэтому больному необходимо создать условия с минимальной возможностью нанесения травм и увечий. Это поможет продлить ему жизнь.
Эффективен ли препарат Аллопуринол при подагре? Читайте отзывы пациентов и мнения врачей.
Процедура иглоукалывание — помощь при грыже позвоночника.
Профилактика
Специфической профилактики фибродисплазии не существует. Люди, имеющие в роду генетическую патологию, перед созданием семьи должны консультироваться в генетических клиниках.
Оссифицирующая фибродисплазия: неминуемая смерть в каменном теле
 Фибродисплазия — заболевание, встречающееся крайне редко и характеризующееся постоянным окостеневанием мягкой скелетной ткани.
Фибродисплазия — заболевание, встречающееся крайне редко и характеризующееся постоянным окостеневанием мягкой скелетной ткани.
Это заболевание затрагивает соединительнотканные слои мышц, апоневрозы, фасции и сухожилия.
Фибродисплазия повсеместно ассоциируется со скелетными аномалиями врождённого характера.
Болезнь характерна вспышкообразными эпизодами напухания в мягких тканях, что влечет за собой их трансформацию в костную ткань.
Что известно о болезни?
Еще сравнительно недавно данная болезнь именовалась в учебной медицинской литературе как «оссифицирующий миозит», болезнь вторичного скелета.
Недавние исследования показали, что такое название не совсем отображает патогенетический исток, сущность болезни ПОФ (прогрессирующая оссифицирующая фибродисплазия).
Данное заболевание вызывает научный интерес уже не первое столетие: сведения о нём собираются с 1648 года, когда в специализированной литературе впервые была упомянута пациентка с окостенением.
Исходя из собранных с тех пор данных, полученных из клинических исследований больных, оссификация, т.е. окостенение скелетных мышц начинается практически сразу же после рождения, причём болезнь распространяется сверху вниз, в такой последовательности:
Болезнь проявляется даже на жевательных мышцах, есть сведения, что пациенты, страдающие их окостенением, умирали вследствие истощения.
Совершенно не важно, когда болезнь проявляется и выходит на пик развития, так как скорость регресса двигательной активности вследствие развития от этого не зависит.
Любое локальное воспаление у носителя фибродисплазии, вне зависимости от причины его появления, вполне вероятно повлечёт за собой начало и дальнейшее прогрессирование болезни.
Проникновение воспалённых клеток в мышечную ткань стимулирует и ускоряет воспалительную стадию нарушения.
В процессе же дозревания, фиброзная ткань участвует в процессе бессосудистого уплотнения, а, превратившись в хрящ, такая ткань уже поступает на стадию остеогенеза и, естественно, вовлекается в процесс характерного для него окостенения.
Стадии развития заболевания
Итак, можно выделить такие стадии прогресса заболевания:

На фото пациенты с диагнозом фибродисплазия
- катализатор, первоначальное, небольшое локальное воспаление;
- прогрессирование болезни и вовлечение в воспалительный процесс тканей вокруг места первого очага;
- стадия бессосудистого уплотнения;
- хрящеобразование;
- стадия остеогенеза и окостенение.
Таким образом, проанализировав стадии патологии, можно утверждать, что разные участки, поражённые болезнью Мюнхеймера с разной скоростью проходят процесс окостенения.
Вместе с тем, несмотря на то, что такое костетворение схоже с процессами образования костей скелета у эмбриона, главное отличие в том, что в первичном скелетообразовании нет воспаления.
Тем не менее, исследователи сходятся на мысли, что эти отличия стоит считать условными, так как доподлинно они не подтверждены из-за того, что биопсия, т.е. взятие образца поражённых участков тела, у таких больных чревата расширением очага заболевания.
Причины заболевания
Факторы, которые способствуют развитию фибродисплазии до сих пор не выяснены, тем не менее, исследователи занимаются активным поиском ответа на этот вопрос.
 Частота врожденных дефектов составляет около 75%.
Частота врожденных дефектов составляет около 75%.
Оссифицирующий миозит рассматривается как всепроникающая болезнь, которой присуща разная степень активности гена.
В преобладающем количестве случаев болезнь бьет точечно, тем не менее, зафиксированы случаи, когда в пределах одной семьи поражены были сразу несколько членов, находящихся в кровном родстве: отец – дети, братья – сестры, и др.
Симптоматика и диагностирование
Два самых явных симптома фибродисплазии:
- воспалительные нарушения в волокнах;
- гетеротопическое костеобразование.
- параартикулярные;
- параоссальные;
- травматические закостенения.
Такая новообразовавшаяся кость и остальная костная ткань в организме не имеют никаких различий.
Костетворение мягких тканей влечёт понижение мышечной силы, прогрессию нарушений дистрофического характера и развитие анкилозов вне суставов.
Нет чёткой схемы, при каких условиях окостенение затрагивает сравнительно небольшие участки, а когда оно заполоняет всё вокруг поражённой области.
Симптомами ПОФ могут послужить как окостенение мягких тканей, так и разнообразные дефекты в развитии.
Наиболее часты такие дефекты как:
- короткопалость большого пальца стопы;
- гипоплазия фаланг, короткий большой палец на кисти;
- клинодактилия в пятом пальце, т.е. его искривленность, скос;
- дефекты позвоночника в шейном отделе;
- расширение и укорочение в шейках бедренных и плечевых костей;
- также есть вероятность глухоты, облысения, гипогонадизма, задержки в развитии.
Нередко нарушение влечёт за собой развитие сколиоза, кривошеи и суставной тугоподвижности.
Заболевание возможно диагностировать лишь после форсированного костеобразования в скелетных тканях, проявляющегося в детском возрасте, от рождения до 13-14 лет.
Наиболее часто болезнь диагностируется на втором с половиной году после начала заболевания. Тем не менее, врождённые аномалии, естественно, обращают на себя внимание сразу же после рождения.
Вовремя диагностировать данное заболевание, увы, практически невозможно. Причина позднего распознавания ПОФ связана, прежде всего, с тем, что врачам и исследователям крайне мало известна этимология патологий вроде аномалии большого пальца стопы.
Генетические исследования
На данном этапе исследования фибродисплазии наиболее важны открытия генетического характера.
Главная находка в этой области – выявление эволюционных изменений BMP4-гена и его РНК, среди клеток у 26 из 32х пациентов с фибродисплазией.
 Таким образом, даже в 21 веке доподлинно не известны гены ПОФ.
Таким образом, даже в 21 веке доподлинно не известны гены ПОФ.
Можно предполагать, причём небезосновательно, что фибродисплазия, диагностированная у пациента, заложена на генетическом уровне.
Также есть вероятность того, что болезнь может быть вызвана сразу несколькими генами, действующими едино.
Как замедлить развитие болезни
В силу того, что причинный фактор развития фибродисплазии не известен, эффективное лечение болезни еще не разработано.
Тем не менее, уже можно выделить определённые препараты, которые замедляют прогресс заболевания.
Выделяется среди прочих препарат Интерферон-g.
Достаточно долгая интерфероновая терапия стимулирует уменьшение мышечных и подкожных инфильтратов. Целесообразно также применение биофосфонатов и этилендиаминтетрауксусной кислоты.
Что же касаемо вторичной профилактики процесса патологии, следует знать, что больным фибродисплазией стоит исключить все вмешательства хирургического характера, инъекции и минимизировать риск травм.
Прогрессирующий оссифицирующий миозит и прогрессирующая оссифипирующая фибродисплазия
Прогрессирующий оссифицирующий миозит (ПОМ) и прогрессирующая оссифицирующая фибродисплазия (ПОФ) представляют собой редкие генетические нарушения остеогенеза. При обоих заболеваниях происходит окостенение мышечной ткани, поэтому четкое разделение данных заболеваний в литературе затруднительно. Зачастую это связано с тем, что авторы используют для этого разные критерии.
Корректное разделение прогрессирующего оссифицирущего миозита и прогрессирующей оссифицирующей фибродисплазии может быть сделано на основании генетических исследований, поэтому в данной работе обзор будет проведен для обоих заболеваний совместно.
Впервые в литературе описание данного заболевания представил Juy Patin в 1692 г., который наблюдал женщину «твердую, как дерево» («dure comme du bois») — вернее было бы сказать, как кость. В XVII I в. еще о 3 больных было доложено в Королевском обществе в Лондоне. К настоящему времени описано около 1000 больных с ПОФ, хотя таких пациентов значительно больше. Каждый ортопед за свою жизнь наблюдает от 2 до 5 больных. Заболевание это настолько редкое, что W.F. Mair (1932), обследовав 130 000 школьников, не обнаружил ни одного, страдающего ПОФ. В 1918 г. это заболевание выявил J. Rosenstirn у лошади и собаки, a H.R. Sciboltal и C.L. Davis (1967) — у свиньи. Скелеты больных ПОМ хранятся в некоторых музеях Великобритании. Название этой болезни дал Von Dusch в 1868 г., а в следующем 1869 г. Miinchmeyer представил описание этого заболевания, основываясь на 12 случаях, и присвоил ему свое имя, что нельзя считать оправданным. J. Rosenstirn в 1918 г. назвал это заболевание «fibrocellulitis ossificans progressiva Fairbank H.»; H. Fairbank в 1950 г. — «fibrosifis ossificans progressiva», К. Banev и W. Bodie в 1940 г., a McKusick в 1960 г. — «fibrodysplasia ossificans progressiva».
L. Lutwak в 1964 г. привел статистические данные, касающиеся 264 случаев.
I. Пол: мужчины — 138; женщины — 117, неизвестен — 9.
II. Локализация первичного процесса: шея — 82, околопозвоночная зона — 46, плечи и руки — 39, голова, лицо, челюсти, таз и ноги — 11, другие — 3, неизвестно — 56.
III. Зона поражения: околопозвоночная зона — 220, плечи и руки — 87, таз и ноги — 103, нижняя челюсть и голова — 72, неизвестно — 20. ПОФ, как правило, сопровождается другой врожденной патологией: укорочением I пальца стопы и I пальца кисти — 87, анкилозом между фалангами пальцев — 149, других пальцев стопы — 17, пальцев кисти — 30, без изменений — 12, неизвестно — 90.
Изменения половых желез и урологические — 11, сердечные — 5, неврологические (синдром Клиппельфейля) — 10.
Возраст, когда обнаружено заболевание: от рождения до 1 года — 57, от 1 года до 2 лет — 22, от 3 до 4 лет — 22, 4—5 лет — 18, 5—6 лет — 14, 6—10 лет — 30, 10—15 лет — 11, 15—20 лет — 8, старше 20 лет — 4, возраст неизвестен — 36. ПОФ наблюдался в 11 семьях, изменения со стороны пальцев были отмечены в 9 из них.
Заболевание ПОМ может начаться еще у плода, но чаще оно начинается в первые годы жизни с окостенения превертебральных мышц, а также мышц, прикрепляющихся к лопатке в области плечевого сустава, трапециевидной мышцы, мышц области тазобедренного сустава, бедра. Обызвествление распространяется вдоль какой-либо мышцы в виде извитой виноградной лозы, которая ветвится, захватывая новые участки. Бывают периоды ремиссии, но потом заболевание опять прогрессирует. Интересно отметить, что не наблюдается обызвествления мышцы сердца, диафрагмы, гортани, языка, сфинктеров и глазных мышц.
Поражаемая мышца сначала отекает, припухает, локально появляется боль, что служит проявлением местных биохимических процессов, затем начинается процесс оссификации и мышцы, апоневрозы, сухожилия окостеневают, а отечность распространяется далее. Скорость, интенсивность процесса различны: у некоторых больных ремиссии длятся годами. Из-за окостенения мышц ограничиваются движения головы, позвоночника, лопаток, крупных суставов, постепенно нарастает инвалидность — к 20—40 и даже к 70 годам. Однако значительная часть больных умирает до 10—20 лет. Смерть наступает обычно из-за окостенения межреберных мышц, мышц брюшной стенки и нарушения дыхания или височной мышцы, мышц нижней челюсти и нарушения жевания, а затем и глотания. Описаны случаи превращения в остеогенную саркому.
В настоящее время исследование ПОФ ведется методами молекулярной биологии, иммунохимии и гистологии. На сегодняшний день известно, что при ПОФ происходит экспрессия генов костных морфогенных белков (BMP) протоонкогенов семейства C-fos/C-jun. Сейчас все большее распространение получает подход, при котором разделяют прогрессирующую оссифицирующую фибродисплазию и прогрессирующий оссифицирующий миозит. Согласно последним исследованиям, необходимо рассматривать остеосаркому как чрезвычайно близкое заболевание.
Как показали работы R.M. Harland (1994), при ПОФ наблюдается гиперэкспрессия мРНК белка BMP 4. Т. Katagivi (1994) установил, что белок BMP 2 вызывает превращение миобластов в остеобласты и что белки BMP являются единственными, которые могут изменять остеогенез при данном заболевании. Они способны превращать in vitro миобласты в минерализованные остеобластоподобные клетки. Проведенные иммунохимические исследования при помощи моноклональных антител не смогли показать различий между белками BMP 2 и BMP 4. Белок BMP 4 включен в разнообразные морфогенные процессы: формирование конечностей, нейрогенез, формирование зубов и другие процессы в раннем эмбриогенезе.
По данным, полученным A. Shafvitz (1998), при ПОФ происходит гиперэкспрессия мРНК BMP 4 и самого белка, при травматическом оссифицирующем миозите — экспрессия белков BMP 1, 4, 6 и c-fos мРНК, а при остеосаркоме — BMP 1—7, c-fos и c-jun мРНК. Таким образом, эти заболевания биохимически очень близки.
В работе Е. Olmsted (1998) было обращено внимание на изучение c-fos семейства протоонкогенов; белок c-fos присутствует в большом количестве в случае остеосаркомы, и его содержание увеличено при ПОФ. Этот белок является компонентом фактора транскрипции АР 1, который регулирует транскрипцию генов и оказывает влияние на развитие конечностей. Сделано также предположение, что ген c-fos служит мишенью для белка BMP 4, но факт регуляции экспрессии не был установлен. При ранней ПОФ нет гиперэкспрессии c-fos; это позволяет предположить, что увеличение уровня c-fos не является причиной возникновения ПОФ. Однако, как уже сказано выше, экспрессия белков BMP 2 и BMP 4 оказывает значительное влияние на процесс развития ПОФ. Интересно также отметить, что экспрессия c-fos и c-jun мРНК происходит скоординированно in vivo и in vitro и что белок BMP 4 ответствен за регуляцию своей экспрессии.
При изучении лимфобластных клеток людей из семей, в которых встречается ПОФ, было установлено, что у них увеличено содержание не только мРНК BMP 4, но и рецепторов сериновых/треониновых киназ, с которыми белок BMP 4 образует гетеромерный комплекс. При этом такое увеличение наблюдалось как у больных ПОФ, так и у здоровых, причем повышение уровня мРНК BMP 4 и самого белка наблюдалось во всех тканях организма, хотя повышение было неодинаковым.
Таким образом, можно сделать вывод, что ген BMP 4 является наиболее вероятной причиной, вызывающей данное заболевание. Тем не менее до сих пор остаются открытыми следующие вопросы: при каких условиях происходит гиперэкспрессия BMP 4, какова молекулярная регуляция гена BMP 4, каким образом клетка воспринимает сигнал белка BMP 4, каков механизм защиты фибробластов кожного покрова и др.
Лечение. Чисто хирургические попытки иссечения части очага у больного с прогрессирующим оссифицирующим миозитом не приводят к успеху. В области оперативного вмешательства нередко очень быстро развивается оссификат еще большего размера.
R. Smith и др. (1976) описали свой опыт лечения 8 больных с прогрессирующим оссифицирующим миозитом. Всем больным они назначали дифосфонат дисодиум этидронат (ЕНДР), пытаясь подавить обызвествление во вновь появляющихся очагах поражения; у 5 из них эктопическая кость была оперативно удалена. ЕНДР иногда замедляет процесс минерализации вновь образованного матрикса после хирургического удаления, однако такое замедление не может быть предсказано. Различный эффект ЕНДР может зависеть частично от величины поглощенного вещества и активности вновь образующейся кости.
R.S. Illingworth (1971) назвал прогрессирующий оссифицирующий миозит ужасным заболеванием, при этом он считал главной целью предотвращение образования в тканях новых очагов обызвествления — окостенения.
Роль кортикостероидов остается далеко не разрешенной. R.S. Illingworth лечил 2 больных, у одного положительного результата не было, у второго ремиссия заболевания, длившаяся 16 лет, позволила автору считать, что кортикостероиды могут играть некоторую роль в лечении прогрессирующего миозита. Он приводит таблицу с отрицательными результатами лечения кортикостероидами у 12 авторов. Лечение гидрокортизоном, трийодтиронином, пропилтиоурацилом не дало положительного результата. Больной, получавший дексаметазон в возрастающих дозах, отмечал улучшение состояния при обострении заболевания, но прогрессирование болезни продолжалось.
С.Т.Зацепин
Костная патология взрослых
Фибродисплазия

- Воспалительные нарушения в волокнах
- Гетеротопическое костеобразование
- Глухота
- Запрокидывание головы назад
- Изогнутость первого пальца стопы вовнутрь
- Искривление позвоночника
- Искривление позвоночника в зоне шеи
- Искривленность пятого пальца
- Короткие большие пальцы на кистях
- Короткие и широкие кости бедра
- Короткие и широкие кости плеча
- Короткий первый палец стопы
- Наклон головы в больную сторону
- Нарушение психического развития
- Отек тканей головы от минимального повреждения
- Отсутствие сустава первого пальца стопы
- Поворот головы
Фибродисплазия (болезнь Мюнхеймера) – это прогрессирующая оссифицирующая редкая генетическая патология, вызванная мутацией гена ACVR1. Заболевание характеризуется врожденными аномалиями строения скелета человека, вызванными окостенениями соединительной ткани, мышц, сухожилий в разных отделах организма.
Прогрессирующая фибродисплазия протекает молниеносно, приводит к серьезным нарушениям опорно-двигательного аппарата, инвалидности и преждевременному летальному исходу. Отмечается чаще у детей в виде болезненных, подобных опухоли, новообразований, которые локализируются в мягких тканях. Со временем они кальцифицируются, что ограничивает подвижность, и в итоге приводит к полному обездвиживанию. Появление таких опухолей может быть вызвано уколами внутримышечно, получениями закрытых травм, хирургическими вмешательствами, однако, болезнь Мюнхеймера может начать развиваться и без весомых причин. Обычно после хирургического удаления новообразований оссифицирующая фибродисплазия продолжает прогрессировать.
Специалистам до настоящего времени не удалось установить точную причину развития прогрессирующей оссифицирующей дисплазии. Происходит самопроизвольная мутация гена, на которую расовые, этнические, географические факторы не оказывают никакого влияния. Из проведенного исследования на близнецах удалось извлечь полезную информацию – факторы окружающей среды имеют разное влияние на развитие аномального явления.
Однако ясно одно: оссифицирующая форма однозначно переходит по наследству в 100% случаев, то есть неизбежно появление потомства с подобной аномалией у больного фибродисплазией.
Развитие патологического состояния можно предупредить своевременной блокировкой мутирующего гена. В большинстве случаев люди с болезнью Мюнхеймера не доживают до зрелого возраста, а многие из тех, кому это удалось, не могут иметь детей в силу аномалии – они бесплодны. Если женщина дожила до репродуктивного возраста, то решиться на роды ей сложно, так как они могут быть для нее смертельными. Также есть переносчики гена ACVR1, которые полностью здоровы, однако? некоторые внешние факторы могут способствовать развитию болезни.
К причинам такого рода можно отнести:
- получение травмы кожного покрова;
- хирургическое вмешательство;
- введение внутримышечных инъекций;
- влияние вирусных заболеваний на человеческий организм.
Реакцией организма на такое заболевание является рост костной ткани в тех местах, где ее быть не должно.
Классификация
Оссифицирующая фибродисплазия классифицируется по стадиям окостенения:
- первая стадия – увеличение количества молодой дегенеративной ткани, появление вторичных дегенеративных изменений в структуре мышцы;
- вторая стадия – происходит развитие атрофии структуры мышцы, рубцевание молодых тканей;
- третья стадия – развитие костной ткани на тех отрезках, где была повреждена мягкая ткань.
Четкие изменения в организме человека явно отображаются на результатах рентгенологических исследований.
Также отличают несколько видов окостенения:
- параартикулярное;
- параоссальное;
- травматическое.
Кости, которые появились таким образом, не имеют отличий от всех остальных костей в организме человека.
Симптоматика
Фибродисплазия не сразу после рождения проявляет себя: первые симптомы можно заметить у ребенка в возрасте от нескольких месяцев до нескольких лет.
Существуют два ярко выраженных симптома болезни Мюнхеймера:
- появление в волокнах воспалительных нарушений;
- гетеротопическое костеобразование.
Также симптоматика может отображать аномалии развития человека или окостенения тканей, например:
- короткий первый палец стопы;
- клинодактилия – отсутствие сустава первого пальца стопы, его изогнутость вовнутрь;
- гипоплазия фаланги, короткие большие пальцы на кистях;
- искривленность пятого пальца;
- отек мягкой ткани головы от минимального повреждения (небольшой ушиб, царапина);
- нарушения в строении позвоночника шейного отдела;
- наличие более широких и коротких костей плеча и бедра;
- не исключается задержка психического развития, глухота, облысение.
Такие заболевания, как сколиоз, кривошея – частое явление при прогрессирующей оссифицирующей фибродисплазии.
Диагностика
Диагностика заболевания не вызывает трудностей и проходит в несколько этапов:
- осмотр пациента;
- генетический анализ крови;
- рентгенологическое исследование.
Описание осмотра зависит от возраста пациента, так как у ребенка 10 лет могут быть замечены небольшие новообразования на любой части тела, а у взрослого человека появляется ограниченность в работе суставов и искривление позвоночника. Такие опухоли уродуют тело человека и не заметить их невозможно.
Генетический анализ не требует специфической подготовки: достаточно сдать кровь натощак, и максимум в течение недели можно получить результаты. При наличии заболевания ученые всегда используют рентгенографический метод исследования, поскольку с его помощью отображаются уплотнения костной структуры. Если же фибродисплазия является ярко выраженной, то за уплотнениями можно и не рассмотреть внутренние органы.
К дифференциальной диагностике относят следующие заболевания:
- прогрессирующая костная гетероплазия;
- остеосаркома;
- лимфедема;
- саркома мягкой ткани;
- десмоидная опухоль;
- агрессивный ювенильный фиброматоз;
- гетеротопная оссификация (наследственная или приобретенная).
Данные методы являются высокоэффективными и позволяют быстро диагностировать наличие аномалии.
Действенного препарата для излечения прогрессирующей оссифицирующей дисплазии до сих пор не обнаружено. Опыты проводятся во всем мире, заболевание изучается, однако, однозначных результатов нет. В мире существует единственный институт, который занимается исключительно этой патологией – лаборатория Маккея.
Одним из действенных препаратов, выявленных учеными, рассматривается Этидронат. Если больной получает большие дозы препарата, заболевание замедляется в развитии. Однако не все так просто: в больших дозировках препарат способен разрушать, помимо новообразовавшейся костной ткани, основной человеческий скелет. Некоторые институты используют препарат с содержанием памидроновой кислоты. Средство действует аналогично этидронату, однако, негативного влияния на скелет человека оказывает в разы меньше.
Остальное лечение имеет цель улучшить состояние пациента во время обострения фибродисплазии, а для этого применяются следующие препараты:
- Преднизолон – оказывает противовоспалительное действие, снимает болевые ощущения, принимать нужно курсом не более двух недель.
- Целебрекс – замедляет воспалительные процессы организма, назначается специалистом, не отпускается без рецепта, так как до конца не изучены побочные действия лекарства.
- Монтелукаст – применяется клиницистами редко, так как действие медикамента до конца не изучено.
- Метаквалон – снижает болевые ощущения при обострении патологии, не подтверждены данные о безопасности препарата, курсы подбираются индивидуально для каждого пациента.

Прием препаратов поможет больным легче справиться с очередной вспышкой заболевания.
Профилактика
Достаточно придерживаться нескольких несложных мер профилактики для того, чтобы максимально приостановить развитие прогрессирующей оссифицирующей фибродисплазии:
- нужно избегать контактов с больными ОРЗ, ОРВИ;
- стараться не получать травмы;
- не переохлаждаться;
- не перегревать организм.
Конечно, гарантия на полное излечение не дается в этом случае, но приостановить развитие заболевания таким способом можно.
Также в плане терапии возможно применение человеческого лейкоцитарного Интерферона, чтобы уменьшить количество подкожных и мышечных инфильтратов.
К большому сожалению, прогноз такого заболевания, как прогрессирующая оссифицирующая фибродисплазия не является благоприятным, так как продолжительность жизни больных очень разнообразна. Все зависит от внешних и внутренних факторов организма.


-0 Комментарий-